Qué es UDI, qué es la Normativa UDI y que relación tiene con GS1
El UDI (Identificador Único del Producto) permite una identificación mundial única de productos sanitarios y, con ello, mejora la seguridad del paciente y los procesos de las empresas del sector salud. Es por eso que GS1 ha sido nombrada entidad emisora del UDI en la Unión Europea. Un sistema único y global de normas es fundamental para permitir una implementación eficaz y efectiva del UDI por parte del sector sanitario en todo el mundo.
El Reglamento europeo sobre los productos sanitarios (“EU MDR”, 2017/745) y el Reglamento europeo sobre los productos sanitarios para diagnóstico in vitro (“EU IVDR”, 2017/746) proporcionan el marco legal para el sistema de identificación única de productos (UDI) dentro de Europa.
La implementación del UDI puede incrementar la seguridad del paciente y mejorar la eficacia de la cadena de suministros sanitarios. Con este sistema, se espera identificar de forma inequívoca los productos sanitarios a lo largo de la cadena de suministros mundial mediante la provisión de información precisa para los profesionales sanitarios y una cadena de suministros mundial y segura, que permita elaborar informes más precisos de acontecimientos adversos, una gestión más eficaz de las campañas de recuperación de productos sanitarios y una reducción de los errores médicos.
En la siguiente tabla se recogen los requisitos normativos del UDI con los códigos equivalentes del Sistema de los Estándares GS1:
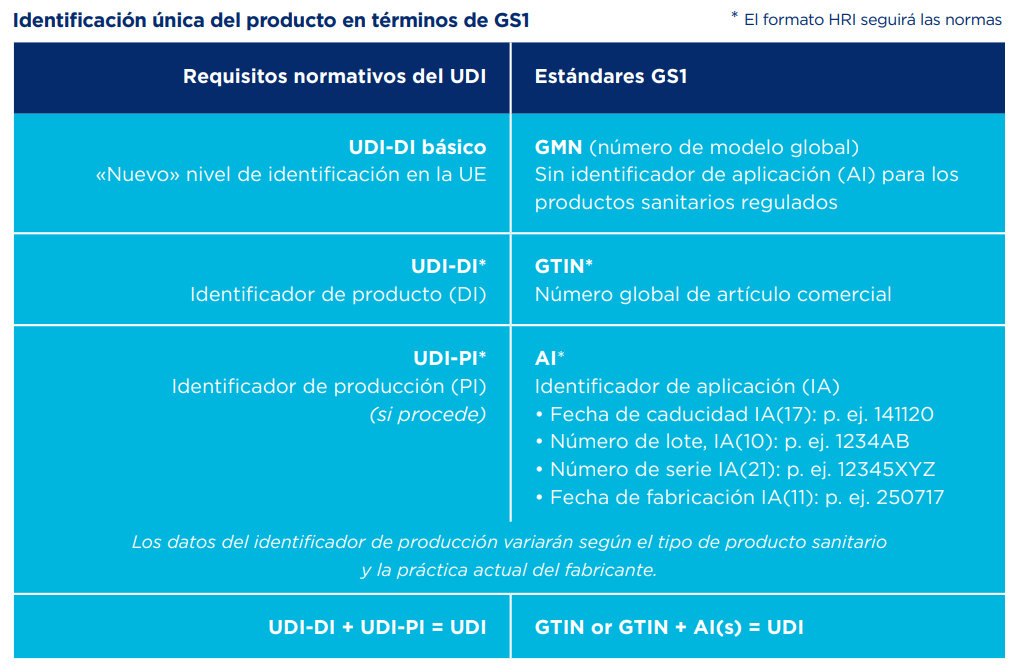
Qué es el UDI-DI Básico y cómo se genera
El UDI-DI Básico o GMN (Número de Modelo Global) es el identificador primario de un modelo/familia/grupo de dispositivos (i.e jeringuilla de insulina, prótesis de cadera…) dentro del portfolio de un fabricante, sin entrar en ninguna variación en características menores o niveles de packaging.
Todos los dispositivos con un mismo Basic UDI-DI deben compartir las mismas características básicas, como uso previsto, clase de riesgo, diseño esencial y características de fabricación.
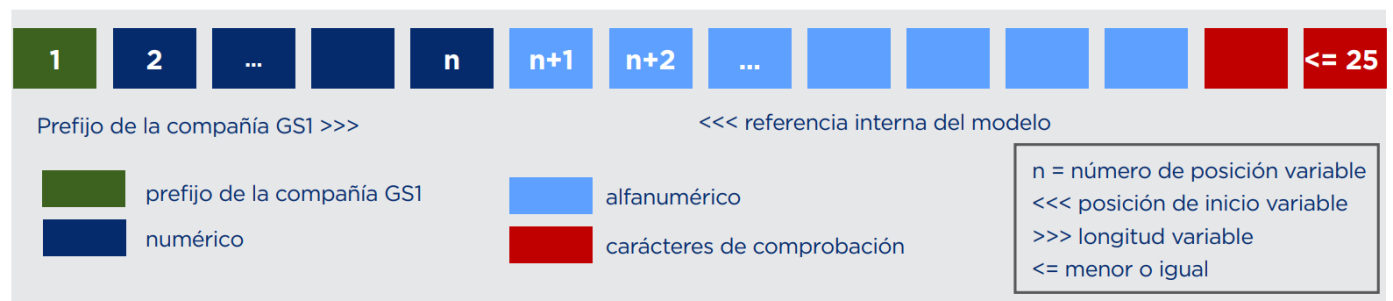
La composición del Basic UDI-DI tiene tres partes:
- Prefijo GS1 de empresa
- Referencia del modelo: designado por la empresa (alfanumérico y distingue mayúsculas y minúsculas)
- Caracteres de control. Se pueden calcular en el generador del GMN
La longitud máxima del UDI-DI Básico contemplando los caracteres de control no debe superar los 25 caracteres.
Qué es el UDI-DI y cómo se genera
El UDI-DI es un identificador de producto sanitario que forma parte de los requisitos normativos del UDI y que equivale a los códigos GTIN . Son numeraciones únicas, universales y no ambiguas que identifican artículos comerciales. GS1 define “artículos comerciales” como productos o servicios que disponen de un precio, se pueden facturar y adquirir en cualquier punto de la cadena de valor.
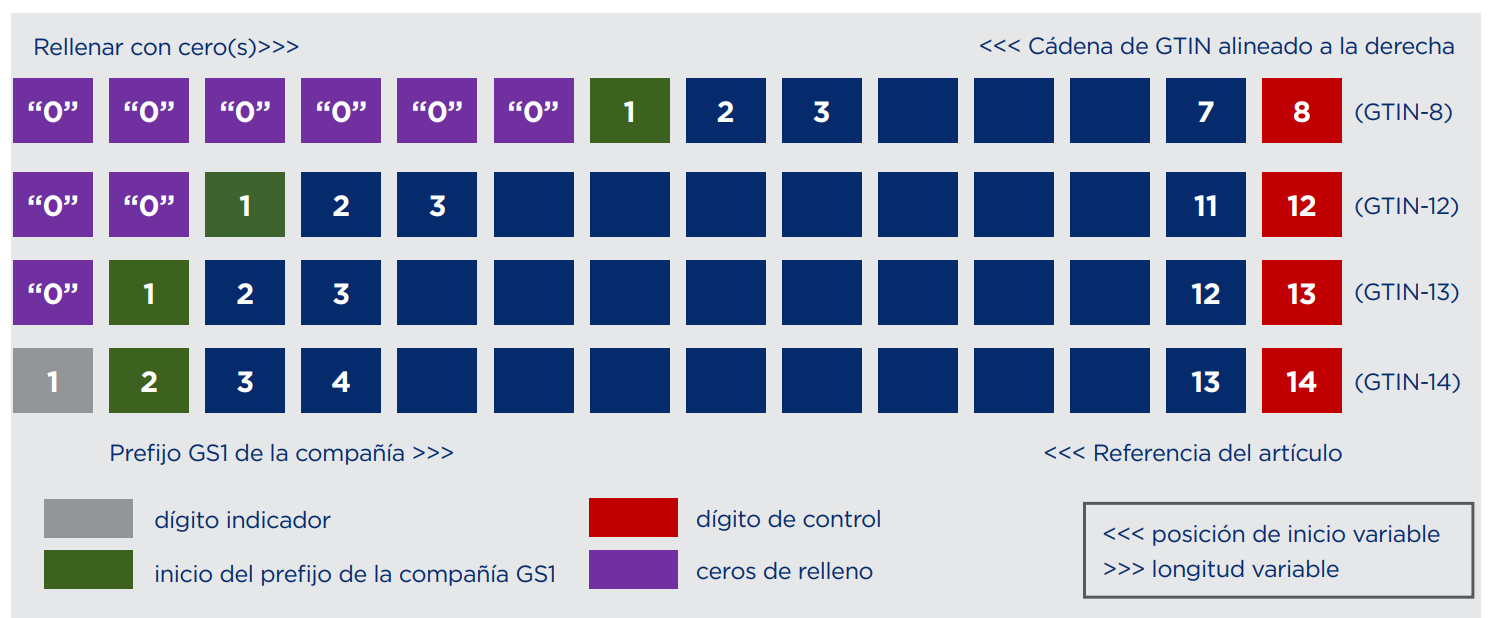
Además, cada GTIN identifica cada formato de producto y a sus respectivas agrupaciones. Los códigos GTIN más utilizados son el GTIN-13 y el GTIN-14 .
Si eres socio de AECOC puedes generar los códigos GTIN, tanto de tus artículos como de tus agrupaciones, desde nuestra plataforma gratuita AECOC ACTIVATE.
Si no eres socio, puedes generar el UDI-DI directamente en el cálculo de dígito de control.
Qué es el UDI-PI y cómo se estructura
En el sistema GS1, el UDI-PI hace referencia a los Identificadores de Aplicación (IA), prefijos numéricos de dos o más dígitos que denotan el tipo y formato de los datos en un código de barras. Cada IA indica qué dato viene a continuación, cómo se estructura y su longitud.
Cada IA está formado por grupos de 2, 3 o 4 caracteres que se representan entre paréntesis. El campo de datos que está identificando siempre está situado a continuación. Dichos datos pueden ser caracteres numéricos y/o alfanuméricos y pueden tener una longitud fija o variable, pudiendo alcanzar una longitud de hasta 30 caracteres en función del IA empleado.
Una de las principales características de estos identificadores es la concatenabilidad, es decir, la posibilidad de unir diversas informaciones en un solo código de barras o símbolo.

Para más información Descarga de la Guía de Codificación y Etiquetado del sector salud
Qué es el AIDC y el HRI UDI
ICAD (Identificación y Captura Automática de Datos) o en inglés AIDC (Automated Identification for Data Capture) es una tecnología utilizada para capturar datos automáticamente. Las tecnologías de ICAD incluyen los códigos de barras, las tarjetas inteligentes, la biometría y la identificación por radiofrecuencia (RFID).
Según el Sistema de Identificación única del dispositivo UDI (Unique device Identification), regulado por la Unión Europea para todos los productos sanitarios, el ICAD haría referencia al código de barras o código bidimensional que se representa en el packaging del producto.
HRI (Human Readable Interpretation) o Interpretación para la lectura humana se refiere a los caracteres impresos debajo, al lado o encima de un código de barras. La HRI es la interpretación legible por las personas de los caracteres codificados en el soporte de la identificación única.
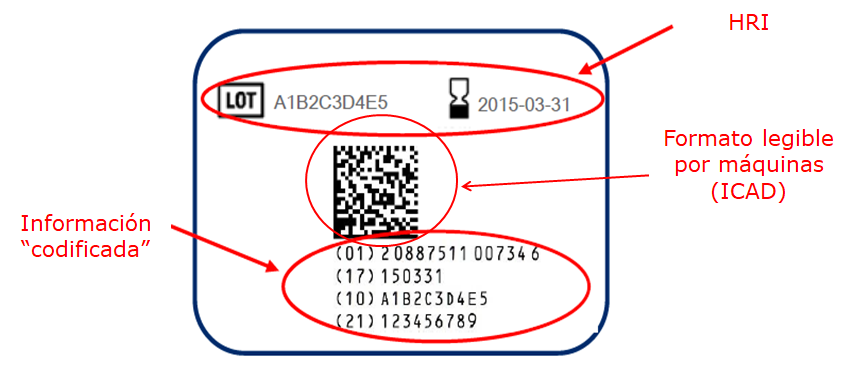
El Reglamento (UE) 2017/745 indica que prevalece la información en ICAD y HRI, si no es posible:
- Prevalece la información en formato ICAD
- Productos destinados a ser utilizados fuera de centros de atención sanitaria (p.e atención domiciliaria), prevalece HRI.
- La información “codificada” es una recomendación de GS1 siempre que exista espacio para ello y no afecte a la correcta lectura de ICAD y HRI.

